朱永建 荆志成
北京协和医院 心内科 & 疑难重症及罕见病国家重点实验室
急性肺栓塞(Pulmonary Embolism, PE)是继急性心肌梗死、脑卒中之后第三位常见致死性心血管疾病。近年来,肺栓塞的发病率和诊断率在全球范围内呈上升趋势,这主要得益于临床医师诊疗意识的提高以及影像学诊断手段的广泛应用等[1]。回顾即将过去的2020年,在突如其来的新冠肺炎疫情的严重影响背景下,肺栓塞领域仍涌现出一批倍受瞩目的重量级研究。
01、美国近10余年肺栓塞死亡率不降反升
一项基于美国和加拿大的死亡原因分析发现[2],加拿大2000~2020年间肺栓塞相关死亡率呈下降趋势,且在2006年后到达平台期。相比之下,美国肺栓塞相关死亡率在2006年止降反升,且这一现象在青年和中年人群中尤为显著。与此同时,另一项研究对美国1999~2018年间肺栓塞死亡原因进行分析,发现2008年以后肺栓塞死亡率明显升高,并且黑人死亡率升高是白人的两倍以上。
尽管发生这一现象的原因仍不清楚,但以上研究结果提示肺栓塞的预防和治疗任重而道远,正如JAMA 2014年发表的社论:肺栓塞百年未解难题。肺栓塞仍需给予持续关注和积极干预[3]。
02、新型冠状病毒肺炎与肺栓塞
新型冠状病毒肺炎(Corona Virus Disease 2019,COVID-19)患者存在高发的血栓并发症风险,这一现象被称为COVID-19相关凝血病。一项纳入18 093例COVID-19患者的荟萃分析发现,静脉血栓栓塞症的发生率为17%,其中肺栓塞发生率为7.1%[4]。而重症COVID-19患者中静脉血栓栓塞症的发生率高达27.9%。肺栓塞的发生与COVID-19患者死亡密切相关[5] 。COVID-19患者血栓形成的潜在机制包括制动、炎症过度激活、病毒介导的高凝状态、细菌混合感染、留置导管和器械以及慢性合并症等。
目前指南推荐,所有无抗凝禁忌证的COVID-19住院患者,均应给予低分子量肝素预防静脉血栓栓塞症。对确诊肺栓塞的患者应规范抗凝治疗,药物包括低分子量肝素、新型口服抗凝药或华法林;重症患者首选胃肠外抗凝;抗凝时程至少三个月[6]。
03、中国肺栓塞先天性易栓症研究
先天性易栓症是指遗传因素导致的血液高凝状态,是静脉血栓栓塞症常见危险因素之一。既往先天性易栓症研究主要针对深静脉血栓形成患者,并没有区分肺栓塞和深静脉血栓形成在发病机制、临床表型及危害性等方面的重要差异。
近期,北京协和医院荆志成教授课题组发表了全球第一项大规模肺栓塞队列的前瞻性研究结果[7] ,该研究连续入选436例急性肺栓塞患者且均进行了先天性易栓症的筛查。结果发现,在中国肺栓塞人群中先天性易栓症的患病比例为7.1%,依次为蛋白S缺乏(3%),蛋白C缺乏(2.8%),抗凝血酶III缺乏(1.1%)(图1)。436例肺栓塞患者中仅1例(0.2%)携带FVL突变,未发现携带PT G20102A突变的患者。研究同时发现,合并先天性易栓症的肺栓塞患者接受长期抗凝治疗,肺栓塞相关死亡或复发风险并未增加。
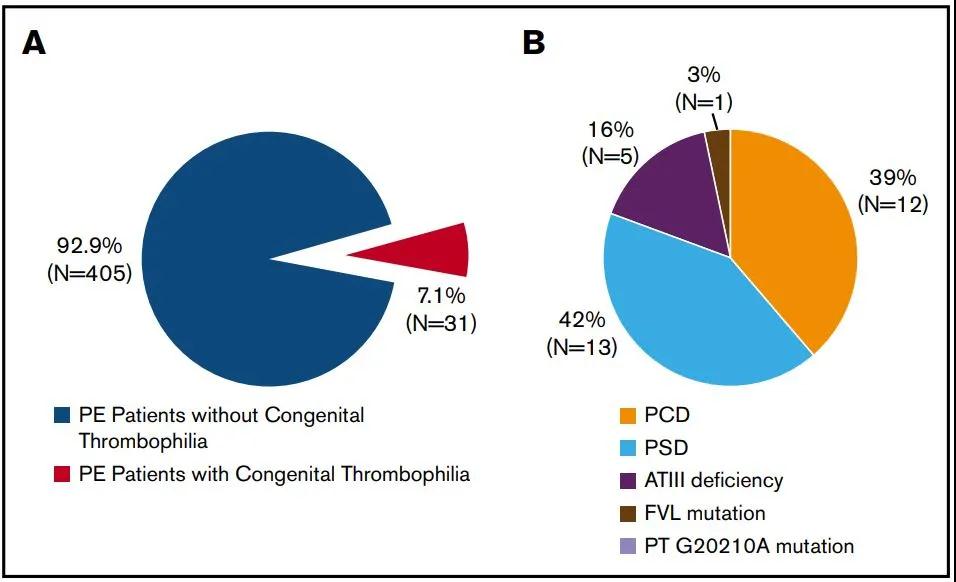
图1. 中国肺栓塞患者中5种先天性易栓症亚型的构成比。(A)先天性易栓症总体构成比;(B)5种亚型的分布比例。
04、抗凝药物研究进展
抗凝治疗是静脉血栓栓塞症治疗的基石,但当前抗凝药物包括新型口服抗凝药的疗效和安全性仍不理想,50%的抗凝治疗患者可能出现血栓后综合征,同时抗凝相关出血仍是较为常见的治疗并发症。
近来研究发现,位于内源性凝血途径上游的XIIa和XIa因子主要参与血栓形成过程而非止血过程,相关靶点抗凝药物可能大大降低患者出血并发症发生率,是极具前景的候选新型抗凝药物[8]。目前在研的XIIa和XIa因子抑制剂包括反义寡核苷酸、单克隆抗体、因子配体及阻断活性位点或诱导变构调节的小分子,其中有三项XI因子抑制剂已进入II期临床试验阶段(表1)。
表1. 目前在研的XIIa和XIa因子抑制剂
05、溶栓治疗现状
尽管多项随机对照试验和荟萃分析证实溶栓是血流动力学不稳定高危肺栓塞的首选治疗策略,但仍缺乏真实世界中溶栓疗效和患者预后的大规模研究证据。
心血管权威期刊European Heart Journal近期发表了德国一项大规模真实世界肺栓塞患者研究,该研究纳入了2005~2015年885 806例德国肺栓塞患者,发现近10年来肺栓塞患者的死亡率呈下降趋势,接受静脉溶栓治疗的比例从2005年的3.1%上升至2015年的4.4%,但仅23.1%血流动力学不稳定的肺栓塞患者接受了溶栓治疗[9]。对于血流动力学不稳定肺栓塞,接受溶栓治疗患者的院内死亡率显著低于未接受溶栓治疗患者(28.6% vs. 49.9%, P <0.001)。
该研究指出,真实世界高危肺栓塞的溶栓治疗仍有较大提升空间,遵循指南溶栓推荐可进一步改善患者的预后。目前我们国家溶栓的真实世界资料不详,相对保守。
06、导管直接溶栓治疗进展
导管直接溶栓是一种导管置入靶向血栓部位进行直接溶栓的治疗方法。既往SEATTLE II研究、FLARE研究以及EXTRACT-PE研究已证实导管直接溶栓治疗肺栓塞的可行性和有效性,但这些研究无一例外采用的是功能学和影像学替代终点,而非死亡等硬终点指标。
近期CHEST杂志发表了基于美国国家再住院数据库的一项研究,结果表明肺栓塞患者经导管直接溶栓的院内死亡率低于全身溶栓(4.5% vs. 17.1%),并且再入院比例也相对降低(7.3% vs. 11.5%)[10]。但考虑到接受全身静脉溶栓患者的病情往往更重,合并休克比例更高,因而研究偏倚较大,仍需前瞻性随机对照研究评估导管直接溶栓的硬终点获益。
此外 SEATTLE II研究的后续分析发现[11],高BMI、肾或肝功能不全、吸烟或基线心率较高是导管直接溶栓治疗后临床指标改善不良的预测因素,这一结果可能有助于筛选从该治疗中潜在获益的肺栓塞患者。
07、外科手术研究进展
外科肺动脉血栓切除术治疗肺栓塞由于其高并发症和高围术期死亡率而饱受争议。近期JACC杂志发表了美国Westchester 医疗中心一组136例(44例大面积肺栓塞,92例高危次大面积肺栓塞)肺栓塞患者接受外科手术或静脉-动脉体外膜肺氧合(Extracorporeal Membrane Oxygenation,ECMO)治疗的研究结果[12],其中23例大面积肺栓塞和91例高危次大面积肺栓塞患者接受单纯肺动脉血栓切除术,19例患者接受ECMO支持治疗(其中3例随后接受肺动脉血栓切除术)。所有患者均获得显著的右室功能改善,仅6例(4.4%)患者围术期死亡。
同期配发的述评指出,该研究结果令人印象深刻,随着治疗经验和生命支持技术的进步,外科治疗正逐渐成为可接受的高危肺栓塞治疗手段。这一研究对后续临床研究的开展和临床应用有重要借鉴价值。
结语
随着胸痛中心在国内的建设推广,本来隐藏在胸痛“隐秘的角落”里的肺栓塞真相,将逐渐被挖掘出来。这个过程需要心脏科、急诊科、血液科、呼吸科以及血管外科和普通内科等所有专科医师高度重视,团结一致,加强开展临床和队列研究。提高我国的肺栓塞诊治水平,降低肺栓塞的发病率和致死率仍然任重而道远。
作者简介
朱永建,北京协和医院心血管内科学博士研究生
▼参考文献
1.Konstantinides SV, Meyer G, Becattini C, Bueno H, Geersing GJ, Harjola VP, Huisman MV, Humbert M, Jennings CS, Jiménez D, Kucher N, Lang IM, Lankeit M, Lorusso R, Mazzolai L, Meneveau N, F N?, Prandoni P, Pruszczyk P, Righini M, Torbicki A, Van Belle E, Zamorano JL. 2019 ESC Guidelines for the diagnosis and management of acute pulmonary embolism developed in collaboration with the European Respiratory Society (ERS). European heart journal 2020; 41(4): 543-603.
2.Barco S, Valerio L, Ageno W, Cohen AT, Goldhaber SZ, Hunt BJ, Iorio A, Jimenez D, Klok FA, Kucher N, Mahmoudpour SH, Middeldorp S, Münzel T, Tagalakis V, Wendelboe AM, Konstantinides SV. Age-sex specific pulmonary embolism-related mortality in the USA and Canada, 2000-18: an analysis of the WHO Mortality Database and of the CDC Multiple Cause of Death database. The Lancet Respiratory medicine 2020.
3.Martin KA, Molsberry R, Cuttica MJ, Desai KR, Schimmel DR, Khan SS. Time Trends in Pulmonary Embolism Mortality Rates in the United States, 1999 to 2018. Journal of the American Heart Association 2020; 9(17): e016784.
4.Jiménez D, García-Sanchez A, Rali P, Muriel A, Bikdeli B, Ruiz-Artacho P, Le Mao R, Rodríguez C, Hunt BJ, Monreal M. Incidence of VTE and Bleeding Among Hospitalized Patients With Coronavirus Disease 2019: A Systematic Review and Meta-analysis. Chest 2020.
5.Scudiero F, Silverio A, Di Maio M, Russo V, Citro R, Personeni D, Cafro A, D’Andrea A, Attena E, Pezzullo S, Canonico ME, Galasso G, Pitì A, Parodi G. Pulmonary embolism in COVID-19 patients: prevalence, predictors and clinical outcome. Thrombosis research 2020; 198: 34-39.
6.Moores LK, Tritschler T, Brosnahan S, Carrier M, Collen JF, Doerschug K, Holley AB, Jimenez D, Le Gal G, Rali P, Wells P. Prevention, Diagnosis, and Treatment of VTE in Patients With Coronavirus Disease 2019: CHEST Guideline and Expert Panel Report. Chest 2020; 158(3): 1143-1163.
7.Lian TY, Lu D, Yan XX, Tan JS, Peng FH, Zhu YJ, Wei YP, Wu T, Sun K, Jiang X, Hua L, Jing ZC. Association between congenital thrombophilia and outcomes in pulmonary embolism patients. Blood advances 2020; 4(23): 5958-5965.
8.Weitz JI, Chan NC. Novel antithrombotic strategies for treatment of venous thromboembolism. Blood 2020; 135(5): 351-359.
9.Keller K, Hobohm L, Ebner M, Kresoja KP, Münzel T, Konstantinides SV, Lankeit M. Trends in thrombolytic treatment and outcomes of acute pulmonary embolism in Germany. European heart journal 2020; 41(4): 522-529.
10.Beyer SE, Shanafelt C, Pinto DS, Weinstein JL, Aronow HD, Weinberg I, Yeh RW, Secemsky EA, Carroll BJ. Utilization and Outcomes of Thrombolytic Therapy for Acute Pulmonary Embolism: A Nationwide Cohort Study. Chest 2020; 157(3): 645-653.
11.Sardar P, Piazza G, Goldhaber SZ, Liu PY, Prabhu W, Soukas P, Aronow HD. Predictors of Treatment Response Following Ultrasound-Facilitated Catheter-Directed Thrombolysis for Submassive and Massive Pulmonary Embolism: A SEATTLE II Substudy. Circulation Cardiovascular interventions 2020; 13(6): e008747.
12.Goldberg JB, Spevack DM, Ahsan S, Rochlani Y, Dutta T, Ohira S, Kai M, Spielvogel D, Lansman S, Malekan R. Survival and Right Ventricular Function After Surgical Management of Acute Pulmonary Embolism. J Am Coll Cardiol 2020; 76(8): 903-911.